ابيضَاض الدَّم النِّقوي الْمُزْمِن
كتبت المقال: رغد هيوتي
دققت المقال: بتول البدور
ابيضاض الدّم النِّقويّ المزمن:
ابيضَاض الدَّم النِّقوي المزمن و يعرف أيضًا بسرطان المُحَبَّبات المزمن و اللوكيميا النخاعيّة المزمنة، هو نوع من أنواع سرطانات الدّم، يتمثّل بنموّ غير طبيعيّ للخلايا الجذعيّة المكوّنة لخلايا الدّم البيضاء، و هو سرطان بطيء النموّ و هذا سبب تسميته بالمزمن. [1]
يصيبُ ابيضَاض الدَّم النِّقوي المزمن جميع الأعمار، وتبلغ حالات الإصابة به 1-2 من كل 100000 عند البالغين،[2] بتركيزٍ أكبر في منتصف الخمسينيّات وما بعدها [3] ولا يصيب إلّا عددًا قليلًا جدًّا من الأطفال.[2]
نخاعُ العظم هو مكان تصنيع الدّم في الجسد، ويضمّ نوعين من الخلايا الجذعيّة التي تنتج منها خلايا الدِّم المتنوّعة كما يظهر في الصورة، وهما[4]:
- (Myeloid cells) – الخلايا النقوّية
- (Lymphoid cells) – الخلايا اللمفاويّة
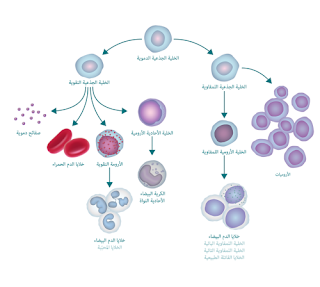
[5]
يحدث ابيضَاض الدَّم النِّقوي المزمن حين تنموّ خلايا الدّم البيضاء النقويّة بشكل ومعدّلٍ غير طبيعيّين، إذ تحتل هذه الخلايا أحيانًا حيّزًا كبيرًا في نخاع العظم يعيق نمو الخلايا الطبيعية ويدفع بالخلايا الجديدة إلى الدّم قبل نضجها.
أسباب تطوّر المرض:
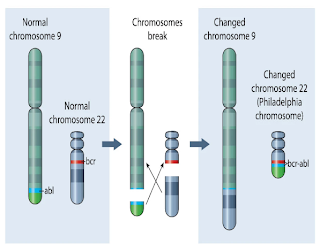
يحدث ابيضاض الدّم النقويّ المزمن نتيجة مشكلة في كروموسومات الخلايا المصابة، إذ تحدث طفرة تبادل بين جزء من كروموسوم رقم ٢٢ و جزء من كروموسوم رقم ٩، ما يؤدّي إلى قِصر الكروموسوم ٢٢ واختلاف صِفاته فيُعطى اسم كروموسوم فيلادليفيا. [6]
تتواجد هذه الطفرة في معظم المصابين بالمرض، وبوجودها يحدثُ اختلافٌ في الجينات يسمّى (BCR-ABL1) يحفّز الخلايا على الانقسام والتكاثر بلا توقّف. [6]
[7]
عوامل الخطورة التي تزيد احتمالية الإصابة:
- التعرّض للإشعاع. [6]
- تقدّم العمر.
- أظهرت بعض الدراسات شيوع ابيضاض الدّم النّقويّ المزمن أكثر لدى الذكور. [8]
تطوّر المرض:
ينقسم ابيضَاض الدَّم النِّقوي المزمن إلى عدّة مراحل متباينة في الأعراض، قد يختلف العلاج باختلافها، وهذه المراحل هي:
- المرحلة المزمنة (chronic phase):
تنمو خلايا الدّم النقويّة ببطءٍ في هذه المرحلة، و قد لا تظهر على المريض أيّة أعراض.[3]
- المرحلة المتسارعة (accelerated phase):
وهي مرحلة انتقالية يشتدّ فيها المرض قبل وصوله للمرحلة النهائيّة، حيث يتسارع نمو الخلايا في هذه المرحلة و قد تظهر على المريض بعض الأعراض. [3]
- المرحلة الأرومية (blast phase):
تتطوّر هذه المرحلة عند معظم المرضى في حال لم يتلقوا العلاج في المرحلة المزمنة، وفيها يتزايد عدد الخلايا غير الناضجة بشكل كبير، وقد تتراكم في أماكن مختلفة من الجسم مثل : الطّحال، الدّماغ، و الكبد، وهذه المرحلة هي الأكثر خطورة إذ تنخفض فيها فرص العلاج و تشتدّ فيها الأعراض. [6]
أعراض المرض:
في المراحل المبكّرة من ابيضَاض الدَّم النِّقوي المزمن لا تكون هناك أعراض واضحةّ عادةً، و قد يتمّ اكتشافه مبكرًا صدفةً، من خلال الفحوصات التي تُجرى لأسباب صحّيّة أخرى، مع تقدّم حالة المريض قد تظهر عليه الأعراض التالية نتيجة لفقر الدّم ونقص المناعة، وتراكم الخلايا السقيمة :
- التعرّق الليليّ. [9]
- فقدان الوزن. [9]
- الشعور بالتّعب .[3]
- شحوب الجلد و ضيق النّفس.[3]
- الشعور بالشبع المبكّر.[3]
- ألم وانتفاخ وامتلاء في الجانب العلويّ والأيسر من البطن (بسبب تضخُّم الطّحال).[3]
- ارتفاع درجة حرارة الجسم. [3]
- الكدمات والنزيف المتكرر من إصابات طفيفة. [3]
- الالتهابات المتكرّرة. [3]
- آلام العظام. [3]
تشخيص ابيضاض الدّم النقويّ المزمن:
يتم تشخيص ابيضاض الدّم النقويّ المزمن من خلال:
- فحوصات الدم المخبريّة والتي تُظهر ارتفاعًا كبيرًا في كريات الدّم البيضاء. [9]
- إجراء اختبار جزيئيّ للكشف عن وجود كروموسوم فيلادلفيا المُحدِّد للمرض. [9]
- أخذ عيّنة من نخاع العظم. [3]
علاج ابيضاض الدّم النقويّ المزمن :
- أدوية تُسمَّى (مثبّطات كيناز التيروسين TKIs).
- المعالجة الكيميائيّة. [10]
- فصادّة الكريات البيضاء ( leukapheresis) وهذه عادةً تُستخدم للحوامل. [10]
- المعالجة بالخلايا الجذعيّة. [10]
مآل المرض :
يعيشُ عدد كبير من المرضى حياة طويلة طبيعيّة بفضل العلاجات الحديثة المتخصّصة، لكنّ ذلك يُحدّد بعدّة عوامل منها[11]:
- حالة المريض عند التشخيص بما في ذلك مرحلة المرض ومدى انتشاره وظهور أيّ من مضاعفاته.
- عمر المريض -إذ يكون المرض أكثر عداونيّة في الأعمار الصغيرة نسبيًا.
- مدى تجاوب المرض وتراجعه مع العلاج.
وعمومًا كلّما كان التشخيص في وقت مبكّر من تطوّر المرض، كانت مآلاته أفضل.
المصادر:
(1) Haznedaroğlu, İbrahim C. et al. “WHO 2016 Definition of Chronic Myeloid Leukemia and Tyrosine Kinase Inhibitors.” Turkish journal of haematology : official journal of Turkish Society of Haematology vol. 37,1 (2020): 42-47. doi:10.4274/tjh.galenos.2019.2019.0241
(2) Jabbour, E., & Kantarjian, H. (2022). Chronic myeloid leukemia: 2022 update on diagnosis, therapy, and monitoring. American journal of hematology, 97(9), 1236–1256. https://doi.org/10.1002/ajh.26642
(3) Eden RE, Coviello JM. Chronic Myelogenous Leukemia. [Updated 2023 Jan 16]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2023 Jan-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK531459/
(4) Lee JY, Hong SH. Hematopoietic Stem Cells and Their Roles in Tissue Regeneration. Int J Stem Cells. 2020 Mar 30;13(1):1-12. doi: 10.15283/ijsc19127. PMID: 31887851; PMCID: PMC7119209.
(5) https://together.stjude.org/ar-sa/about-pediatric-cancer/types/leukemia.html
(6) Rinaldi, Ikhwan, and Kevin Winston. “Chronic Myeloid Leukemia, from Pathophysiology to Treatment-Free Remission: A Narrative Literature Review.” Journal of blood medicinevol. 14 261-277. 6 Apr. 2023, doi:10.2147/JBM.S38209
(7) PDQ Pediatric Treatment Editorial Board. Childhood Acute Lymphoblastic Leukemia Treatment (PDQ®): Health Professional Version. 2015 Sep 28. In: PDQ Cancer Information Summaries [Internet]. Bethesda (MD): National Cancer Institute (US); 2002-. Available from: https://www.ncbi.nlm.nih.gov/books/NBK65763.2/
(8) Ning, Liqing et al. “Trends in disease burden of chronic myeloid leukemia at the global, regional, and national levels: a population-based epidemiologic study.” Experimental hematology & oncology vol. 9,1 29. 3 Nov. 2020, doi:10.1186/s40164-020-00185-z
(9) Thompson, Philip A et al. “Diagnosis and Treatment of Chronic Myeloid Leukemia in 2015.” Mayo Clinic proceedings vol. 90,10 (2015): 1440-54. doi:10.1016/j.mayocp.2015.08.010
(10) Aladağ, Elifcan, and İbrahim Celalettin Haznedaroğlu. “Current perspectives for the treatment of chronic myeloid leukemia.” Turkish journal of medical sciences vol. 49,1 1-10. 11 Feb. 2019, doi:10.3906/sag-1810-81
(11) Iezza, M., Cortesi, S., Ottaviani, E., Mancini, M., Venturi, C., Monaldi, C., … Castagnetti, F. (2023). Prognosis in Chronic Myeloid Leukemia: Baseline Factors, Dynamic Risk Assessment and Novel Insights. Cells, 12(13), 1703. https://doi.org/10.3390/cells12131703

Leave a Reply
Want to join the discussion?Feel free to contribute!